30 Nov 22
Geschätzte Lesezeit:min
Aider le foie à se régénérer : une piste prometteuse pour des patients condamnés
Satdarshan (Paul) Singh Monga, University of Pittsburgh Health SciencesLe foie est bien connu pour sa capacité à se régénérer, inégalée parmi les organes du corps humain. Il peut en effet se reconstituer complètement même après ablation chirurgicale des deux tiers de sa masse. Mais les dommages causés par certains médicaments, l’abus d’alcool ou l’obésité peuvent finir par provoquer sa défaillance…
Actuellement, le seul traitement efficace de l’insuffisance hépatique au stade terminal est la transplantation.
Malheureusement, comme pour beaucoup d’autres organes, il y a une pénurie de greffons disponibles. Selon leur compatibilité, les malades doivent attendre de 30 jours à plus de cinq ans avant de recevoir un foie aux États-Unis. Sur les plus de 11 600 patients inscrits sur liste d’attente pour recevoir une greffe de foie en 2021, un peu plus de 9 200 seulement en ont bénéficié. (En France, en 2020, 1 128 greffes de foie ont été réalisées. Chaque année, près de 10 % des malades en liste d’attente vont « soit décéder en liste d’attente, soit sortir de la liste en raison de leur état de santé trop dégradé avant de décéder. Il y a actuellement plus de deux candidats en attente d’une greffe de foie pour un greffon disponible », ndlr)
Mais que se passerait-il si, au lieu d’une transplantation de foie, il existait un traitement capable d’aider le foie à développer encore ses capacités de régénération ?
Je suis le directeur fondateur du Centre de recherche sur le foie de Pittsburgh et je dirige un laboratoire étudiant la régénération du foie et le cancer. Dans nos travaux récemment publiés, mon équipe et moi avons découvert que l’activation d’une catégorie de protéines particulière à l’aide d’un nouveau médicament peut contribuer à accélérer la régénération et la réparation du foie après une grave lésion ou après une ablation chirurgicale partielle chez la souris.
Acteurs clefs dans la régénération
Le foie remplit plus de 500 fonctions fondamentales dans notre organisme. Il intervient notamment dans le tri des nutriments reçus de l’intestin, qu’il transforme, traite, etc. pour générer énergie, hormones et autres molécules qui seront nécessaires dans tout le corps. Il produit ainsi des protéines qui transportent les graisses, gère la conversion de l’excès de glucose en glycogène pour le stocker, le cholestérol, l’élimination de toxines comme l’ammoniac, le métabolisme des certains médicaments, etc.
Les cellules hépatiques, ou hépatocytes, assument ces nombreuses tâches grâce à une stratégie géographique dite de « zonation ». Chaque unité fonctionnelle du foie est orientée par le flux sanguin traversant l’organe, ce qui permet de le diviser en trois zones fonctionnellement distinctes. Les cellules acquièrent une différentiation particulière selon leur localisation et elles vont activer des fonctions spécialisées distinctes dans chaque zone en activant des gènes spécifiques. Cependant, malgré des pistes pour expliquer cette « zonation métabolique », on ne sait pas encore exactement ce qui contrôle l’expression de ces gènes.
Au cours des deux dernières décennies, mon équipe et d’autres laboratoires ont identifié un groupe de 19 protéines appelées Wnts qui jouent un rôle important dans le contrôle des fonctions et de la régénération du foie. Nous savons désormais que les protéines Wnt contribuent à activer le processus de réparation des cellules hépatiques endommagées… mais celles qui contrôlent réellement la zonation et la régénération, ainsi que leur emplacement exact dans le foie, restent un mystère.
Pour identifier ces protéines et leur origine, mon équipe et moi-même avons utilisé une nouvelle technologie appelée cartographie moléculaire pour déterminer où sont activés cent gènes connus pour leurs implications dans les fonctions hépatiques, et l’intensité de cette activité.
De façon inattendue, nous avons constaté que seuls deux des 19 gènes Wnt, Wnt2 et Wnt9b, étaient fonctionnellement présents dans le foie. Nous avons également trouvé que tous deux étaient actifs dans les cellules endothéliales qui tapissent les vaisseaux sanguins de la zone 3 du foie – une zone qui joue un rôle dans nombre de fonctions métaboliques.
À notre grande surprise, l’élimination de ces deux gènes Wnt a abouti à ce que toutes les cellules hépatiques n’expriment que des gènes généralement limités à la zone 1, limitant ainsi considérablement le fonctionnement global de l’organe. Cette découverte suggère deux choses : que les cellules hépatiques subissent une influence continue sur l’activation de leurs gènes, qui peut donc être modifiée ; et que Wnt est le régulateur principal de ce processus.
L’élimination des deux gènes Wnt des cellules endothéliales a également complètement stoppé la division des cellules du foie, et donc sa capacité de régénération après une ablation chirurgicale partielle.
Premiers tests d’efficacité
Étant donné qu’ils contribuent à la fois à la zonation et la régénération, ces gènes constituent une voie prometteuse pour le développement de médicaments en médecine régénérative. Nous avons alors décidé de tester si une nouvelle molécule, un anticorps appelé FL6.13 (créé par ingénierie protéique selon la technique du rational design) pourrait aider à restaurer ces deux fonctions primordiales.
Cette molécule s’est avérée capable de se fixer sur des récepteurs spécifiques aux protéines Wnt. Elle pourrait donc en effet partager des fonctions similaires avec elles, notamment l’activation de la faculté de régénération de l’organe.
Pendant deux jours, nous avons administré cet anticorps à des souris génétiquement modifiées pour que les cellules endothéliales de leur foie n’expriment ni Wnt2 ni Wnt9b. Nous avons établi que cette molécule était capable de rétablir presque complètement les fonctions de division et de réparation des cellules hépatiques.
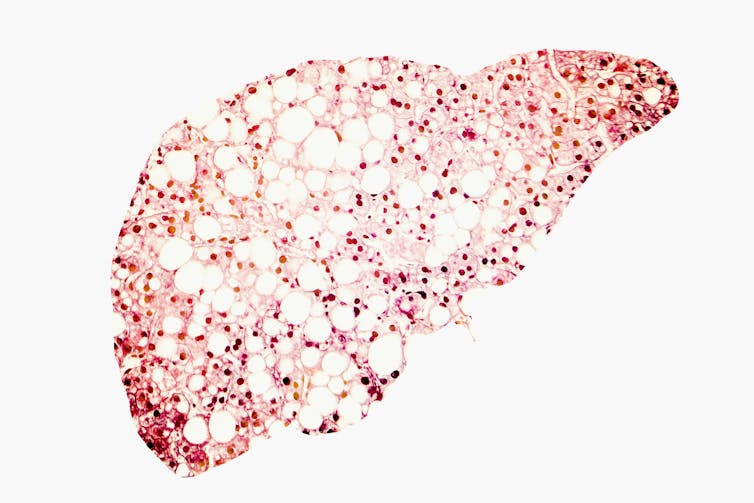
Pour aller plus loin, nous avons voulu tester l’efficacité de ce médicament potentiel pour réparer le foie après une surdose de paracétamol. Le paracétamol, ou acétaminophène dans la nomenclature internationale, est le médicament en vente libre le plus couramment utilisé pour traiter la fièvre et la douleur. Cependant, pris en quantité trop importante, il peut causer de graves dommages au foie.
Sans soins médicaux immédiats, cette surdose peut entraîner une insuffisance hépatique et la mort. L’empoisonnement au paracétamol est ainsi l’une des causes les plus fréquentes de lésions hépatiques graves nécessitant une transplantation du foie aux États-Unis notamment. Malgré cela, il n’existe actuellement qu’un seul médicament pour le traiter et il n’est capable de prévenir les lésions hépatiques que s’il est pris très rapidement après le surdosage.
[Près de 80 000 lecteurs font confiance à la newsletter de The Conversation pour mieux comprendre les grands enjeux du monde. Abonnez-vous aujourd’hui]
Nous avons testé notre anticorps sur des souris présentant des lésions hépatiques dues à des quantités toxiques de paracétamol. De façon encourageante, nos analyses ont montré qu’une seule dose permettait de diminuer les biomarqueurs sanguins de lésions – des protéines que le foie libère lorsqu’il est lésé – et de réduire la mort des tissus hépatiques. Ces résultats indiquent que tant la réparation des cellules hépatiques que la régénération des tissus ont lieu.
Réduire le besoin en transplantation
Une façon de remédier à la pénurie de greffes de foie serait d’améliorer les traitements des maladies du foie. Si les médicaments actuels peuvent traiter l’hépatite C, une infection virale qui provoque une inflammation du foie parfois bénigne mais potentiellement responsable de cirrhoses et cancers, d’autres atteintes de cet organe majeur n’ont pas connu les mêmes progrès.
Il existe ainsi très peu de traitements efficaces pour des maladies comme la stéatose hépatique non alcoolique ou la maladie alcoolique du foie, ce qui fait que l’état de nombreux patients s’aggrave irrémédiablement. Ces derniers finissent alors par avoir besoin d’une greffe. Une opération, on l’a vu, qui manque cruellement de greffon disponible.
Mon équipe et moi-même pensons qu’en améliorant encore la capacité du foie à se réparer lui-même, on pourrait éviter le recours à la transplantation dans certains cas. Notre étude est un premier pas préliminaire qui montre que des possibilités existent. Des recherches complémentaires plus approfondies sur les capacités de notre anticorps FL6.13 comme l’élaboration de nouvelles molécules capables de favoriser la régénération du foie ouvrent quoiqu’il en soit déjà des pistes inédites contre le fléau des atteintes hépatiques graves.![]()
Satdarshan (Paul) Singh Monga, Professor of Pathology and Medicine, University of Pittsburgh Health Sciences
Nous remercions l'auteur et The Conversation pour l'autorisation de republication.
